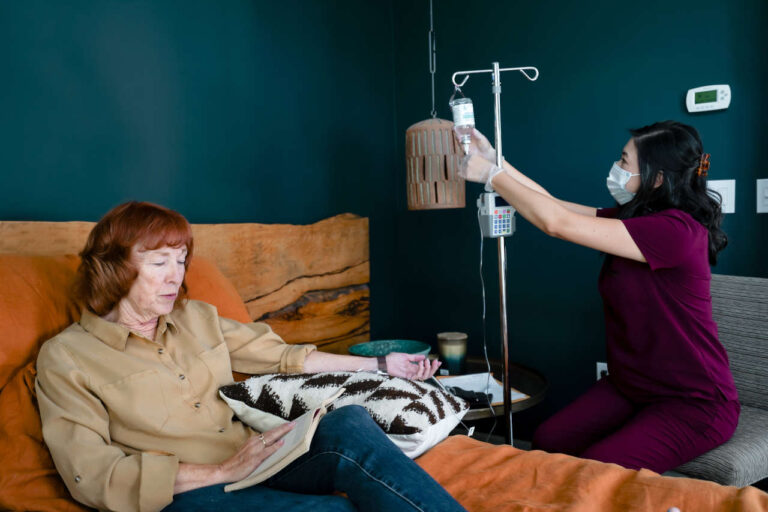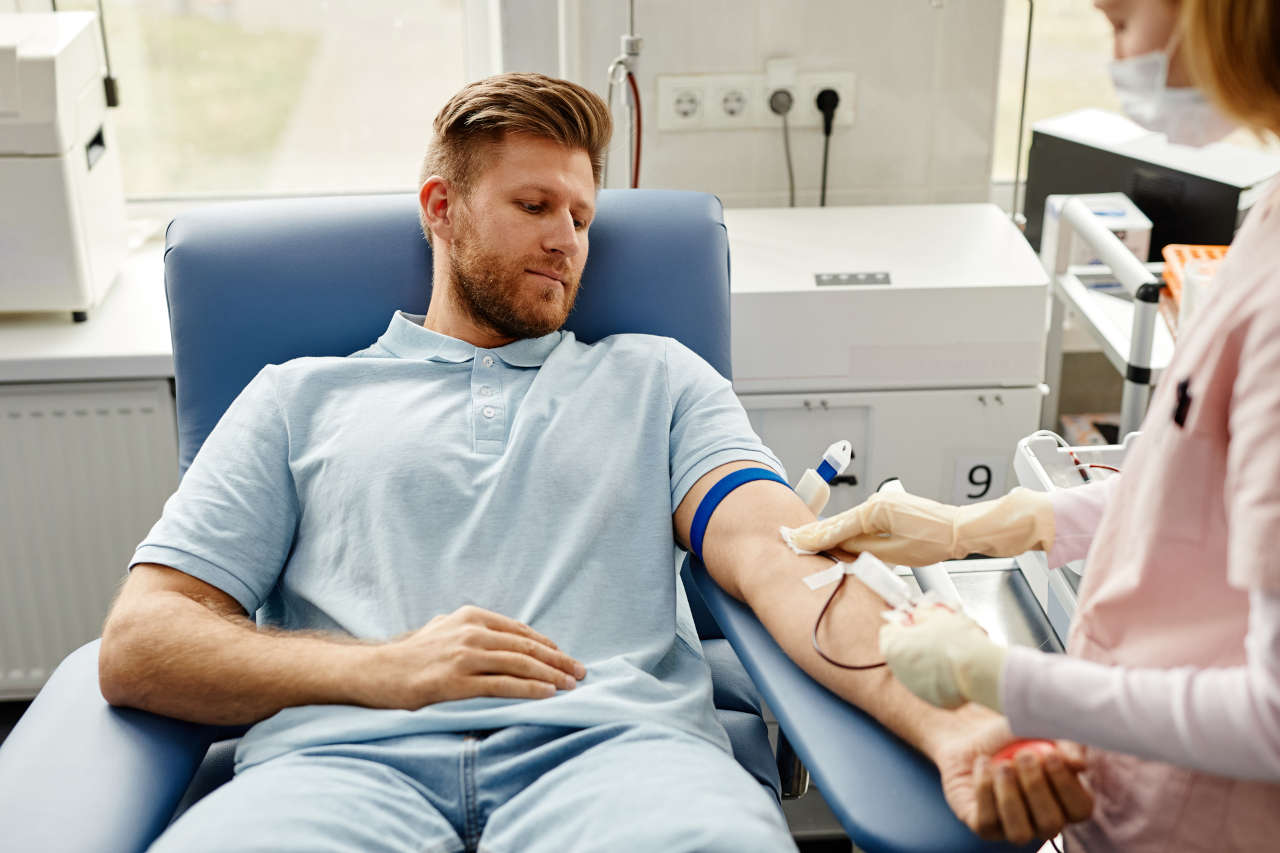
Globulin miễn dịch tiêm tĩnh mạch (IVIG) là một sản phẩm điều trị được điều chế từ huyết tương của hàng ngàn người hiến tặng. Huyết tương người chứa nhiều thành phần thiết yếu, bao gồm immunoglobulin (Ig), còn được gọi là kháng thể. Globulin miễn dịch là thành phần quan trọng của hệ thống miễn dịch và giúp cơ thể chống lại nhiễm trùng.
Hỏi về dịch truyền IVIG tại nhà
Quá trình tinh chế immunoglobulin từ huyết tương để tạo ra liệu pháp điều trị cho bệnh nhân rất phức tạp và tốn thời gian. Phải mất khoảng 9 tháng để sản xuất một lô sản phẩm IVIG phục vụ mục đích điều trị.
Sản phẩm IVIG cuối cùng bao gồm hỗn hợp kháng thể được tiêm tĩnh mạch vào máu của bệnh nhân.
Trong bài viết này, chúng tôi sẽ thảo luận về một loạt các bước mà mọi nhà sản xuất đều tuân theo để tạo ra dung dịch IVIG vô trùng cuối cùng phục vụ mục đích điều trị.
Quy trình sản xuất IVIG
Các bước liên quan đến quá trình sản xuất IVIG bao gồm thu thập huyết tương, phân đoạn, tinh chế, bào chế, thử nghiệm và đóng gói.
Thu thập huyết tương
Quy trình sản xuất IVIG bắt đầu bằng việc thu thập huyết tương từ hàng ngàn người hiến tặng khỏe mạnh. Người hiến tặng được lựa chọn thông qua sàng lọc nghiêm ngặt để đảm bảo chất lượng và độ an toàn cao nhất của huyết tương.
Huyết tương được sử dụng để sản xuất IVIG được lấy từ hai nguồn: Khoảng 20% đến từ những người hiến máu, trong khi phần còn lại 80% có nguồn gốc từ người hiến huyết tương.
Vì immunoglobulin chỉ chiếm một phần nhỏ trong huyết tương, nên cần rất nhiều lần hiến tặng để sản xuất đủ IVIG điều trị cho bệnh nhân. Ví dụ, để sản xuất đủ IG điều trị cho một bệnh nhân suy giảm miễn dịch trong một năm, cần khoảng 130 lần hiến tặng từ những người khỏe mạnh.
Phân đoạn huyết tương
Sau khi thu thập huyết tương, một loạt các quá trình phân đoạn diễn ra, trong đó các protein huyết tương như globulin miễn dịch, các yếu tố đông máu và albumin được tách ra khỏi các thành phần plasma khác.
Kỹ thuật phân đoạn của Cohn, được phát triển bởi Edwin J. Cohn trong Thế chiến II, phương pháp này thường được thực hiện, với một số cải tiến mới hơn, để chiết xuất dung dịch immunoglobulin cô đặc từ huyết tương. Trong kỹ thuật này, một lượng nhỏ cồn (ethanol) được sử dụng để giảm độ pH và cường độ ion nhằm tách albumin và các protein huyết tương khác dựa trên độ hòa tan của chúng.
Trong quá trình này, nhiệt độ được giữ ở mức thấp để giảm khả năng nhiễm bẩn và cho phép phân đoạn ở quy mô lớn.
Thanh lọc IVIG
Sau khi các globulin miễn dịch được tách bằng phương pháp phân đoạn, quá trình tinh chế nghiêm ngặt được thực hiện để tạo ra dung dịch globulin miễn dịch cô đặc. Quá trình tinh chế loại bỏ các protein không hoạt động, tạp chất và chất gây ô nhiễm khỏi dung dịch. Để tinh chế globulin miễn dịch, cần có các phương pháp khác nhau. sắc ký các phương pháp như sắc ký trao đổi ion sử dụng DEAE Sephadex®, sắc ký cảm ứng điện tích kỵ nước và sắc ký loại trừ kích thước được sử dụng.
Mỗi kỹ thuật sắc ký là duy nhất và mang lại 95% – 97% của IgG tinh khiết cao từ thể tích nhỏ huyết tương người trong quy trình tinh chế một bước. Ví dụ, sắc ký cột DEAE Sephadex® tạo ra dung dịch IgG 95% có độ tinh khiết cao.
Ngược lại, sắc ký loại trừ kích thước giúp tách các dạng immunoglobulin IgG khác nhau dựa trên kích thước tương ứng của chúng khỏi huyết tương gộp.
Hơn nữa, các quy trình sắc ký còn giúp loại bỏ immunoglobulin IgA, có thể gây sốc phản vệ nghiêm trọng ở những bệnh nhân thiếu hụt IgA và có kháng thể anti IgA trong máu.
Loại bỏ các tác nhân gây bệnh có hại
Vì IVIG được tạo thành từ các nhóm huyết tương từ hàng ngàn người hiến tặng, nên có khả năng một loại vi-rút như HIV hoặc Viêm gan C có thể được chứa trong mẫu. Mặc dù việc lựa chọn người hiến IVIG được thực hiện rất cẩn thận bằng cách sàng lọc người hiến và kiểm tra mẫu hiến để tìm virus hoặc vi khuẩn, nhưng việc sử dụng quy trình phân đoạn là rất quan trọng để đạt được độ tinh khiết cao trong mẫu.
Ngoài ra, một số phương pháp được thiết kế để loại bỏ hoặc vô hiệu hóa các tác nhân gây bệnh do vi-rút như sau:
- Xử lý bằng dung môi/chất tẩy rửa (S/D) vô hiệu hóa vi-rút bằng cách sử dụng các hóa chất phá hủy lớp vỏ ngoài của chúng.
- Thanh trùng là quá trình đun nóng dung dịch IVIG đến 60℃ trong 10 giờ.
- Bức xạ UVC và bức xạ liều thấp phương pháp được sử dụng để tiêu diệt vi-rút bằng cách tấn công vào cấu trúc di truyền của nó.
- Xử lý pH thấp phá vỡ lớp bảo vệ của vi-rút và thay đổi cấu trúc protein.
- Lọc nano là một loại phương pháp siêu lọc trong đó dung dịch IVIG đi qua màng (bộ lọc) có các lỗ quá nhỏ để vi-rút có thể lọt qua.
IVIG có thể giúp ích gì? | Thông tin điều trị IVIG miễn phí
Công thức và thành phần của IVIG
Sau khi IVIG được tinh chế, nó trải qua quá trình điều chế và ổn định để đảm bảo hiệu quả và độ ổn định. Các nhà sản xuất điều chế và ổn định dung dịch IVIG bằng cách điều chỉnh độ pH và thêm các chất ổn định như đường hoặc axit amin. Bước này làm cho mỗi sản phẩm IVIG khác nhau về công thức và thành phần.
Kiểm tra và đóng gói cuối cùng của IVIG
Các sản phẩm IVIG trải qua quy trình kiểm tra và kiểm soát chất lượng nghiêm ngặt trong suốt quá trình sản xuất. Nhiều xét nghiệm và phân tích được thực hiện để loại bỏ các chất gây ô nhiễm, mầm bệnh virus hoặc prion.
Sau khi hoàn tất các thử nghiệm kiểm soát chất lượng, sản phẩm cuối cùng được chuyển vào lọ trong môi trường vô trùng và ủ trong vài tuần để đảm bảo chất lượng và độ an toàn cao.
Sau khi kiểm tra lần cuối, IVIG được dán nhãn, đóng gói và chuyển đến các cơ sở chăm sóc sức khỏe để sử dụng trong điều trị.
Phần kết luận
IVIG được sản xuất từ huyết tương của hàng ngàn người hiến tặng, sau đó được tinh chế thông qua các phương pháp tinh chế và kiểm soát chất lượng nghiêm ngặt. Từ khâu thu thập huyết tương đến pha chế dung dịch IVIG vô trùng, quy trình thu thập được tuân thủ nghiêm ngặt ở mọi bước để đảm bảo tính an toàn, hiệu quả và chất lượng của sản phẩm.
TÀI LIỆU THAM KHẢO:
- Barahona Afonso, AF, & Pires João, CM (2016). Quy trình sản xuất và tác dụng sinh học của Globulin miễn dịch tiêm tĩnh mạch. Các phân tử sinh học, 6(1). https://doi.org/10.3390/biom6010015
- Durandy, A., Kaveri, SV, Kuijpers, TW, Basta, M., Miescher, S., Ravetch, JV, & Rieben, R. (2009). Globulin miễn dịch tiêm tĩnh mạch – tìm hiểu đặc tính và cơ chế. Miễn dịch học lâm sàng và thực nghiệm, 158(Phụ lục 1), 2-13. https://doi.org/10.1111/j.1365-2249.2009.04022.x
- Knezevic-Maramica, I., & Kruskall, MS (2003). Globulin miễn dịch tiêm tĩnh mạch: Cập nhật cho bác sĩ lâm sàng. Truyền máu, 43(10), 1460-1480. https://doi.org/10.1046/j.1537-2995.2003.00519.x
- Cowden, J., & Parker, SK (2006). Globulin miễn dịch tiêm tĩnh mạch: sản xuất, công dụng và tác dụng phụ. Tạp chí Bệnh truyền nhiễm Nhi khoa, 25(7), 641-642. 10.1097/01.inf.0000223517.98486.2f