Xembify es un tipo de inmunoglobulina subcutánea (IGSC). Contiene un amplio espectro de anticuerpos (inmunoglobulinas) extraídas de una gran cantidad de plasma humano.
Xembify es una solución de inmunoglobulina 20% que está indicado por la FDA para la inmunodeficiencia humoral primaria y se puede utilizar en una variedad de otras afecciones médicas.
Obtenga su dosis de Xembify
Habla con un especialista¿Qué hay dentro de Xembify?
Xembify es un producto estéril, apirógeno y listo para usar. La solución contiene IgG (proteína 18-22%) presente en glicina de 0,16 M a 0,26 M y alrededor de 10 – 40 mcg/ml de polisorbato.
Xembify no contiene ningún conservante y no está fabricado con látex de caucho.
¿Cómo se ve?
Xembify es una solución incolora a amarillo pálido, casi transparente o ligeramente opalescente.
¿Cómo funciona Xembify?
Xembify proporciona una variedad de inmunoglobulinas (Ig) Que son opsonizantes (más fáciles de destruir) y neutralizantes por naturaleza. Las bacterias, virus, parásitos y agentes micoplasmáticos, así como las toxinas que liberan, son neutralizados por los anticuerpos presentes en Xembify.
Xembify Asistencia para copagos
Almacenamiento Xembify
El Xembify se conserva refrigerado (entre 2 y 8 grados Celsius). También se puede conservar a temperatura ambiente hasta 6 meses, antes de la fecha de caducidad. No congelar.
Si se refrigera, deje que el Xembify alcance la temperatura ambiente antes de usarlo. No lo caliente en el microondas.
Tratamiento/Terapia
Xembify está indicado por la FDA para la inmunodeficiencia humoral primaria en pacientes de 2 años o más. Esto incluye, entre otros, agammaglobulinemia congénita, inmunodeficiencia común variable (IDCV), agammaglobulinemia ligada al cromosoma X, síndrome de Wiskott-Aldrich e inmunodeficiencias combinadas graves.
Inmunodeficiencia humoral primaria (IP)
La función subóptima del sistema inmunológico en un inmunodeficiencia humoral primaria El paciente puede ser perjudicial. El tratamiento con Xembify puede fortalecer considerablemente el sistema inmunitario y mejorar la calidad de vida.
Contraindicaciones
Si bien el Xembify tiene un amplio margen de tolerancia y aceptación, aún existen casos en los que su administración está contraindicada. Algunas de estas condiciones se mencionan a continuación.
Reacción alérgica
No se debe administrar Xembify a candidatos que hayan presentado una reacción anafiláctica o alérgica grave a las inmunoglobulinas humanas. Las principales manifestaciones de esta reacción de hipersensibilidad incluyen:
- Dificultad para respirar
- Hinchazón en la zona del cuello
- Erupción cutánea grave
- Acrocianosis (extremidades que se tornan azules)
Debe buscar atención médica de inmediato si comienzan a aparecer los síntomas mencionados anteriormente.
Si ha experimentado problemas similares anteriormente con IgIV, entonces no debes utilizar Xembify.
Deficiencia de IgA
Debes mantenerte alejado de Xembify o cualquier otro inmunoglobulina Infusión si tiene deficiencia de IgA. Esto se debe a que las personas con deficiencia de IgA suelen desarrollar anticuerpos anti-IgA. Por lo tanto, el cuerpo responde con una reacción de hipersensibilidad, que en ocasiones puede ser mortal.
Infusión subcutánea
A diferencia de Terapias con IgIV, que se administran por vía intravenosa, Xembify se administra únicamente por vía subcutánea.
Dosificación
La farmacocinética y la respuesta clínica del paciente determinan la dosis de Xembify. Se adopta la siguiente secuencia para determinar la dosis correcta.
- Después de iniciar el tratamiento con Xembify, mida el nivel mínimo de IgG sérica del paciente a las 5 semanas.
- Continúe monitoreando el nivel mínimo de IgG cada 2 a 3 meses para determinar si es necesario realizar ajustes de dosis posteriores.
- Para dosificaciones frecuentes (es decir, de dos a siete veces por semana), divida la dosis semanal calculada por la cantidad deseada de infusiones por semana.
Nota: Si un paciente no mantiene una respuesta clínica adecuada al tratamiento con Xembify (o no alcanza el nivel sérico de IgG de un tratamiento previo), podría ser necesario ajustar la dosis. Para ello, el médico calculará la diferencia entre el nivel mínimo de IgG y el nivel mínimo de IgG objetivo y, a continuación, determinará la diferencia mediante la siguiente tabla:
Ajuste de dosis (ml por semana)
| Diferencia con el nivel valle de IgG objetivo (mg/dl) | 10 kilos | 15 kilos | 20 kilos | 30 kilos | 40 kilos | 50 kilos | 60 kilos | 70 kilos | 80 kilos | 90 kilos | 100 kilos | 110 kilos | 120 kilos |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 50 | 0 | 1 | 1 | 1 | 2 | 2 | 2 | 3 | 3 | 3 | 4 | 4 | 5 |
| 100 | 1 | 1 | 2 | 2 | 3 | 4 | 5 | 5 | 6 | 7 | 8 | 8 | 9 |
| 150 | 1 | 2 | 2 | 3 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 13 | 14 |
| 200 | 2 | 2 | 3 | 5 | 6 | 8 | 9 | 11 | 12 | 14 | 15 | 17 | 18 |
| 250 | 2 | 3 | 4 | 6 | 8 | 9 | 11 | 13 | 15 | 17 | 19 | 21 | 23 |
| 300 | 2 | 3 | 5 | 7 | 9 | 11 | 13 | 16 | 18 | 20 | 23 | 25 | 27 |
| 350 | 3 | 4 | 5 | 8 | 11 | 13 | 16 | 19 | 21 | 24 | 27 | 29 | 32 |
| 400 | 3 | 5 | 6 | 9 | 12 | 15 | 18 | 21 | 24 | 27 | 30 | 33 | 36 |
| 450 | 3 | 5 | 7 | 10 | 14 | 17 | 20 | 24 | 27 | 31 | 34 | 38 | 41 |
| 500 | 4 | 6 | 8 | 11 | 15 | 19 | 23 | 27 | 30 | 34 | 38 | 42 | 45 |
Localice la cantidad correspondiente (en ml) en la que debe aumentar/disminuir la dosis semanal en función del peso corporal del paciente.
Ejemplo: Si un paciente con un peso corporal de 70 kg tiene un nivel mínimo de IgG de 900 mg/dl y el nivel objetivo es de 1000 mg/dl, la diferencia es de 100 mg/dl. Por lo tanto, aumente la dosis semanal en 5 ml.
Administración segura de Xembify
Obtener autorización previa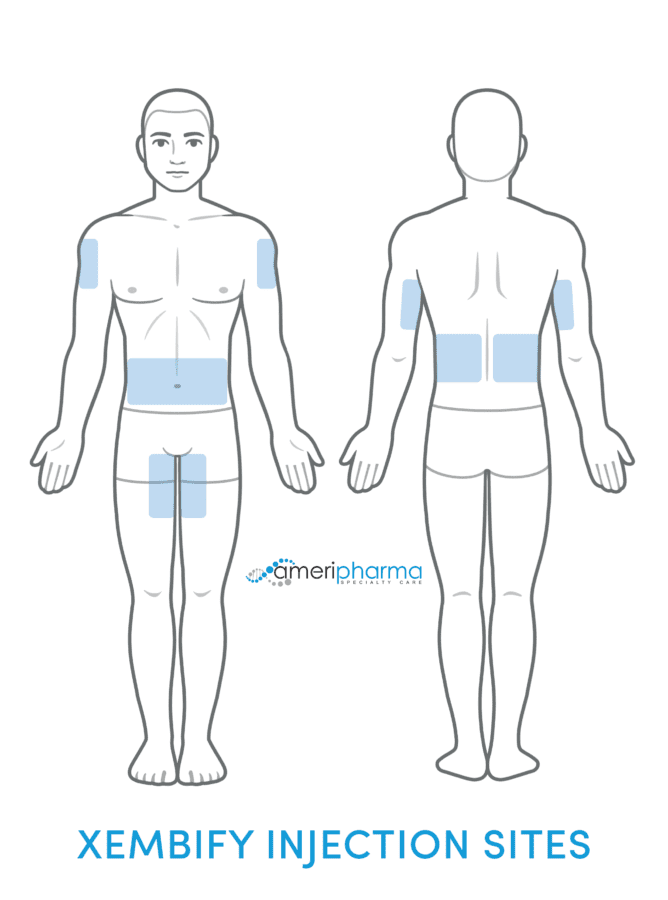
Precauciones
Embarazo
No existen datos disponibles en humanos que indiquen la presencia o ausencia de riesgo asociado al fármaco. No se han realizado estudios de reproducción en animales con Xembify. Se desconoce si puede causar daño fetal al administrarse a mujeres embarazadas o si puede afectar la capacidad reproductiva.
Madres lactantes
No existen datos en humanos que indiquen la presencia o ausencia de riesgo asociado al fármaco. Se deben considerar los beneficios de la lactancia materna para el desarrollo y la salud, junto con la necesidad clínica de la madre de Xembify y cualquier posible efecto adverso en el lactante.
Uso pediátrico
El Xembify se evaluó en 14 pacientes pediátricos (de 2 a 16 años) con IP en un ensayo clínico multicéntrico. Los perfiles de seguridad y eficacia fueron similares a los de los pacientes adultos. No se requirió una dosis específica pediátrica para alcanzar los niveles séricos de IgG deseados. No se ha establecido la seguridad ni la eficacia del Xembify en pacientes pediátricos menores de 2 años.
Uso geriátrico
Los estudios clínicos de Xembify no incluyeron un número suficiente de sujetos mayores de 65 años para determinar si responden de forma diferente a la de sujetos más jóvenes. Tres sujetos del estudio incluidos en el ensayo clínico tenían 65 años o más. En general, la selección de la dosis para un paciente de edad avanzada debe hacerse con precaución, comenzando generalmente con la dosis más baja del rango.
Costo
El costo de Xembify es de alrededor de $188 para un suministro de 5 ml.
Obtenga su dosis de IgIV
Infusión en casaAsistencia para copagos
Programas de asistencia para copagos Están disponibles para Xembify, donde los pacientes elegibles pueden pagar $0. Los programas ofrecen asistencia con el copago que varía entre $5,000 y $10,000 al año.
El paciente deberá presentar una solicitud para ver si cumple con los criterios para recibir asistencia con el copago.
Advertencias sobre el uso de Xembify
Tras una evaluación, su médico determinará si Xembify es ideal para usted. Informe a su médico si:
- Tiene problemas cardiovasculares (del corazón)
- Sufre de hiperviscosidad (espesura) de la sangre debido a un estilo de vida sedentario.
- Tener un catéter intravenoso permanente colocado
- ¿Está tomando algún medicamento que contenga estrógeno?
- Tiene insuficiencia renal (de los riñones)
- Tiene factores de riesgo de trombosis
Los pacientes con riesgo de trombosis deben ser tratados con extrema precaución. En estos casos, el médico puede prescribir Xembify a una dosis mínima y una velocidad de infusión menor.
Advertencias y precauciones
Reacciones de hipersensibilidad
Pueden producirse reacciones de hipersensibilidad graves en humanos. inmunoglobulina Productos, incluido Xembify. Si se produce una reacción de hipersensibilidad, suspenda inmediatamente la infusión de Xembify y administre el tratamiento adecuado.
Xembify contiene IgA. Los pacientes con anticuerpos anti-IgA conocidos tienen un mayor riesgo de desarrollar hipersensibilidad potencialmente grave o reacciones anafilácticas. Xembify está contraindicado en pacientes con deficiencia de IgA, anticuerpos contra IgA y antecedentes de hipersensibilidad al tratamiento con inmunoglobulina humana.
Trombosis
Puede producirse trombosis después del tratamiento con productos de inmunoglobulina, incluido Xembify.
Factores de riesgo:
- Edad avanzada
- Inmovilización prolongada
- Condiciones de hipercoagulabilidad
- Historia de trombosis venosa/arterial
- Uso de estrógenos
- Catéteres vasculares centrales permanentes
- Hiperviscosidad
- Factores cardiovasculares
La trombosis puede ocurrir en ausencia de factores de riesgo conocidos.
Considere la evaluación basal de la viscosidad sanguínea en pacientes con riesgo de hiperviscosidad, incluidos aquellos con crioglobulinas, quilomicronemia en ayunas/triglicéridos marcadamente altos o gammapatías monoclonales. Para pacientes con riesgo de trombosis, administrar Xembify a la dosis mínima y velocidad de infusión posible.
Asegúrese de que los pacientes estén bien hidratados antes de la administración. Vigile la presencia de signos y síntomas de trombosis y evalúe la viscosidad sanguínea en pacientes con riesgo de hiperviscosidad.
Síndrome de meningitis aséptica (SMA)
Se ha reportado AMS con el uso de inmunoglobulina humana administrada por vía intravenosa y subcutánea. Generalmente comienza entre varias horas y dos días después del tratamiento con inmunoglobulina. El AMS puede presentarse con mayor frecuencia en mujeres que en hombres.
Síntomas:
- Dolor de cabeza severo
- Rigidez de nuca (rigidez del cuello)
- Modorra
- Fiebre
- Fotofobia (sensibilidad a la luz)
- Movimientos oculares dolorosos
- Náuseas
- Vómitos
Los estudios del líquido cefalorraquídeo (LCR) con frecuencia muestran pleocitosis de hasta varios miles de células por milímetro cúbico, predominantemente de la serie granulocítica, y niveles elevados de proteínas de hasta varios cientos de mg/dl, pero los resultados del cultivo son negativos.
Para descartar otras causas de meningitis, se debe realizar un examen neurológico completo a los pacientes que presenten síntomas, incluidos estudios de LCR.
El AMS puede presentarse con mayor frecuencia en asociación con dosis altas (>2 g/kg) o infusión rápida de inmunoglobulinas. La interrupción del tratamiento con inmunoglobulinas ha resultado en la remisión del AMS en pocos días sin secuelas.
Obtenga asistencia para el copago de IgIV
Asistencia financiera para la IgIVInsuficiencia renal y hemólisis
El uso de inmunoglobulinas humanas, especialmente las que contienen sacarosa, puede causar disfunción/insuficiencia renal aguda, necrosis tubular aguda, nefropatía tubular proximal, nefrosis osmótica y la muerte. Xembify no contiene sacarosa. Asegúrese de que los pacientes no presenten depleción de volumen antes de la administración de Xembify.
Pacientes en riesgo
Los pacientes con riesgo de desarrollar disfunción renal incluyen pacientes con cualquier grado de insuficiencia renal preexistente o predisposición a insuficiencia renal aguda, como:
- Diabetes mellitus
- Mayor de 65 años
- Depleción de volumen
- Septicemia
- Paraproteinemia
- Recibir fármacos nefrotóxicos conocidos
Para estos pacientes, controlar la función renal y considerar dosis más bajas y frecuentes.
La monitorización periódica de la función renal y la diuresis es especialmente importante en pacientes con un riesgo potencial mayor de desarrollar insuficiencia renal aguda. Evaluar la función renal, incluyendo la medición de... nitrógeno ureico en sangre (BUN)/creatinina sérica, antes de la infusión inicial y, posteriormente, a intervalos adecuados. Si la función renal se deteriora, considere suspender el tratamiento con Xembify.
Hemólisis
Los productos de IgG, incluido el Xembify, pueden contener anticuerpos de grupos sanguíneos que pueden actuar como hemolisinas e inducir el recubrimiento in vivo de los glóbulos rojos (GR) con inmunoglobulina, lo que provoca un resultado positivo en la prueba de antiglobulina directa (Coombs) y hemólisis. Tras la terapia con inmunoglobulina humana, puede desarrollarse anemia hemolítica tardía debido al aumento del secuestro de GR, y se ha reportado hemólisis aguda compatible con hemólisis intravascular.
Monitorizar a los receptores de Xembify para detectar signos y síntomas clínicos de hemólisis, especialmente en pacientes con factores de riesgo como un grupo sanguíneo distinto del O o pacientes que reciben dosis altas de IgG (≥ 2 g/kg). Los estados inflamatorios subyacentes en un paciente pueden aumentar el riesgo de hemólisis, pero su papel es incierto.
Si hay signos y/o síntomas de hemólisis después de la infusión de Xembify, realice pruebas de laboratorio confirmatorias apropiadas.
Lesión pulmonar aguda relacionada con la transfusión (TRALI)
Tras el tratamiento con inmunoglobulinas humanas, puede presentarse edema pulmonar no cardiogénico en pacientes. La TRALI se caracteriza por dificultad respiratoria grave, edema pulmonar, hipoxemia, función ventricular izquierda normal y fiebre. Los síntomas suelen presentarse entre 1 y 6 horas después del tratamiento.
Monitorizar a los pacientes para detectar reacciones adversas pulmonares. Si se sospecha TRALI, realizar las pruebas pertinentes para detectar la presencia de anticuerpos antineutrófilos y anti-HLA tanto en el producto como en el suero del paciente. La TRALI puede controlarse mediante oxigenoterapia con soporte ventilatorio.
Interferencia con las pruebas de laboratorio
Tras la infusión de Xembify, el aumento transitorio de diversos anticuerpos transferidos pasivamente en la sangre del paciente puede producir resultados serológicos falsos positivos, con el riesgo de una interpretación errónea. Asegúrese de informar a su médico sobre su tratamiento.
Transmisión de agentes infecciosos
Dado que la Xembify se elabora a partir de sangre humana, puede conllevar el riesgo de transmitir agentes infecciosos (es decir, virus), el agente de la enfermedad de Creutzfeldt-Jakob variante (vECJ) y el agente de la enfermedad de Creutzfeldt-Jakob (ECJ). Esto también aplica a virus desconocidos o emergentes y otros patógenos.
No se han reportado casos de transmisión de ECJ ni de ninguna otra enfermedad viral con el uso de Xembify.
Efectos secundarios no graves
Las reacciones locales a la administración de Xembify incluyen:
- Eritema (enrojecimiento) en el lugar de la infusión
- Dolor en el lugar de la infusión
- Hinchazón del lugar de la infusión
- hematomas en el lugar de la infusión
- Prurito (picazón) en el lugar de la infusión
- Induración (firmeza) del lugar de infusión
- Costra en el lugar de la infusión
- Edema en el lugar de la infusión
- Reacciones sistémicas (por ejemplo, tos y diarrea)
Las reacciones adversas más comunes en más del 5% de los sujetos del ensayo clínico fueron reacciones adversas locales.
Pregúntele a un especialista en IgIV sobre los efectos secundarios
Interacciones farmacológicas
Vacunas de virus vivos atenuados
La transferencia pasiva de anticuerpos puede interferir transitoriamente con la respuesta inmune del cuerpo a las vacunas de virus vivos como:
- Paperas
- Sarampión
- Rubéola
- Varicela
Debe informar a su proveedor de atención médica sobre cualquier terapia reciente con Xembify antes de vacunarse para que se puedan tomar las medidas de precaución adecuadas.
Pruebas serológicas
Varios anticuerpos transferidos pasivamente en preparaciones de inmunoglobulina, incluido Xembify, pueden confundir los resultados de las pruebas serológicas.